Prof. Dr. Thorsten Jungmann (Stand 2025-10-23)
Eine Batterie ist ein nicht wiederaufladbarer elektrochemischer Energiespeicher (Primärzelle oder Kombination mehrerer Primärzellen). Im Gegensatz zum Akkumulator (Sekundärzelle) kann sie nach Entladung nicht wieder in den Ausgangszustand versetzt werden.
1 Wie sieht sie aus?
Ein zylindrisches, rechteckiges oder flaches Gehäuse aus Metall oder Kunststoff. Häufig mit zwei deutlich markierten Anschlüssen (+/−) und Angaben zu Spannung, Kapazität, Chemietyp und Hersteller. Beispiele: AA-, AAA-, C-, D-, 9V-Block, Knopfzellen.

2 Was kann sie?
Speichert elektrische Energie chemisch und gibt sie bei Bedarf über einen definierten Zeitraum ab. Wird nach Entladung entsorgt oder recycelt.
Die „Kapazität“ (technisch korrekt wäre der Begriff Ladung) einer Batterie wird üblicherweise in Amperestunden (Ah) angegeben. Eine Amperestunde entspricht 3600 Coulomb (C) elektrischer Ladung. Um dies zu veranschaulichen: Eine typische Alkali-Batterie mit einer „Kapazität“ von 2,5 Ah könnte theoretisch einen Strom von 1 Ampere für 2,5 Stunden liefern, bevor sie erschöpft ist.
3 Wie funktioniert sie?
Im Betrieb läuft innerhalb der Zelle an der Anode (–) eine Oxidation ab (Elektronen werden abgegeben), an der Kathode (+) findet eine Reduktion statt (Elektronen werden aufgenommen). Im angeschlossenen Stromkreis fließen die Elektronen vom Minuspol (–) zum Pluspol (+).
Bekannte chemische Systeme sind z. B. Zink-Kohle, Alkaline (Zink-Manganoxid), Lithium-Mangandioxid.
4 Wie sieht sie von innen aus?
Eine Batterie besteht aus einer oder mehreren in Reihe geschalteten Primärzellen. Die Zellen bestehen aus Elektroden und Elektrolyt. Je nach Bauform sind die Elektroden Stäbe, Folien oder Platten. Zwischen den Elektroden befindet sich der Elektrolyt, der den Ionenfluss ermöglicht. Das Gehäuse dient dem Zusammenhalt der Zellen, sowie als Schutz vor mechanischen Einwirkungen und dem Austritt von Elektrolyt.
Auch Batterien besitzen einen kleinen Innenwiderstand, der zu Spannungsabfall und Leistungsverlust führt – dieser steigt mit der Entladung und dem Alter der Batterie an.
GÄNGIGE TECHNOLOGIEN
1. Alkali-Mangan-Batterien
- Bestandteile: Anode aus Zinkpulver und Kathode aus Braunstein (Mangandioxid).
- Eigenschaften: Gute Energiedichte, lange Lagerfähigkeit und eine hohe Belastbarkeit bei mittleren bis hohen Strömen.
- Anwendungsbereiche: Fernbedienungen, Spielzeuge, Taschenlampen und viele andere Haushaltsgeräte. Sie sind der Standard für die meisten AA- und AAA-Batterien.
2. Zink-Kohle-Batterien
- Bestandteile: Zinkbecher als Anode und ein Kohlestab umgeben von einem Mangandioxid-Pulver als Kathode.
- Eigenschaften: Günstig in der Herstellung, aber deutlich geringere Energiedichte und Leistungsabgabe als Alkali-Mangan-Batterien.
- Anwendungsbereiche: Einfache Geräte mit geringem Stromverbrauch, wie zum Beispiel Uhren oder einfache Taschenlampen.
3. Lithium-Primärzellen
Diese Familie von Batterien zeichnet sich durch eine sehr hohe Energiedichte und lange Lagerfähigkeit aus.
- Lithium-Eisendisulfid (Li-FeS2):
- Eigenschaften: Hohe Energiedichte und Leistungsfähigkeit, gute Leistung bei niedrigen Temperaturen.
- Anwendungsbereiche: Handheld-GPS-Geräte, Kamera-Blitzgeräte und andere Geräte, die kurzfristig hohe Ströme benötigen.
- Lithium-Mangandioxid (Li-MnO2):
- Eigenschaften: Hohe Energiedichte und stabiler Betrieb über einen weiten Temperaturbereich.
- Anwendungsbereiche: Typische Knopfzellen für Uhren, Taschenrechner oder Autoschlüssel.
- Lithium-Thionylchlorid (Li-SOCl2):
- Eigenschaften: Außergewöhnlich lange Lagerfähigkeit und hohe Energiedichte. Sie sind für geringe bis mittlere Ströme optimiert.
- Anwendungsbereiche: Industrielle Anwendungen, wie drahtlose Sensoren, Messgeräte oder Notfallausrüstung.
4. Silberoxid-Batterien
- Bestandteile: Anode aus Zink, Kathode aus Silberoxid.
- Eigenschaften: Hohe und sehr stabile Spannungslage, gute Kapazität und hohe Sicherheit.
- Anwendungsbereiche: Hochwertige Armbanduhren und andere präzise elektronische Kleingeräte.
5. Zink-Luft-Batterien
- Bestandteile: Anode aus Zink und eine luftdurchlässige Kathode, die Sauerstoff aus der Umgebungsluft aufnimmt.
- Eigenschaften: Sehr hohe Energiedichte. Sie werden oft erst durch den Kontakt mit der Luft aktiviert.
- Anwendungsbereiche: Hörgeräte, da sie eine kleine Bauform und hohe Kapazität kombinieren.
5 Welche Rolle spielt sie in der Lehre?
Die Batterie dient als Beispiel für eine Spannungsquelle mit begrenzter Lebensdauer. In der Elektrotechnik wird sie oft als reale Spannungsquelle, also ideale Spannungsquelle mit zusätzlichem Innenwiderstand modelliert.
Sie eignet sich für Versuche und Gedankenexperimente mit einfacher Spannungsversorgung, bei denen keine Ladezyklen erforderlich sind.
6 Welche Rolle spielt sie in der Praxis?
Batterien sind weit verbreitet in Geräten mit geringem bis mittlerem Energiebedarf, z. B. Fernbedienungen, Wanduhren, Taschenlampen, medizinische Geräte. Sie sind beliebt, weil sie einfach handhabbar, lange lagerfähig und nahezu wartungsfrei sind.
Symbolik
- Kennbuchstabe in Schaltplänen: G
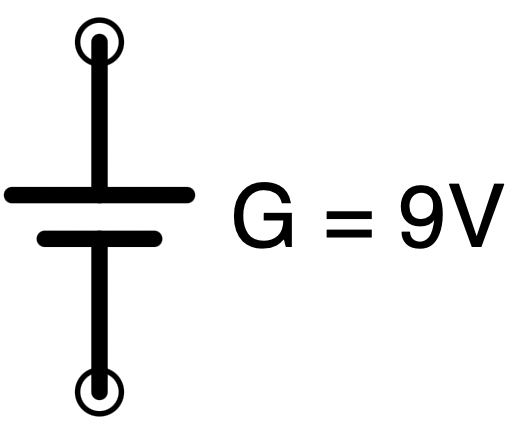
Die Markierung an den Anschlüssen (Kringel) und die Darstellung der Spannung sind nicht standardisiert. Hier gehören sie zur Darstellung in iCircuit.
Die Batterie kann auch als einfache Gleichstromquelle dargestellt werden:

Oder schlicht als ideale Spannungsquelle (wenn die sonstigen Eigenschaften nicht relevant sind):
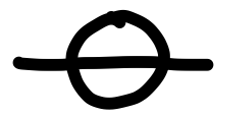
Berechnungen
- Ladung
- Entladen
- Innenwiderstand
